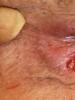
Egy éves hatékony felszámolási program kombinációja. Sémák a helicobacter pylori felszámolására. A Helicobacter pylori felszámolásának indikációi
E. A. J. Rose és R. W. M. Kholst
Modern irányzatok a Helicobacter pylori felszámolásában peptikus fekélybetegségben
Akadémiai Orvosi Központ, Gasztroenterológiai és Hepatológiai Osztály, Amszterdam, Hollandia
A gyomorsavszekréció farmakológiai elnyomása hagyományosan a legracionálisabb megközelítés a fekélyek sikeres kezelésében. Ugyanakkor az antiszekréciós terápiával kezdetben gyógyuló fekélyek hajlamosak a kezelés abbahagyása után kiújulni. Ez a tendencia egyértelműen megváltozik a Helicobacter pylori eradikációja után. Antimikrobiális kezelésben kell részesíteni minden olyan beteget, akinek dokumentált, H. pylori fertőzéssel összefüggő gyomor- és nyombélbetegsége van.
A H. pylori eradikációjának optimális terápiás rendje még mindig nem teljesen meghatározott. A monoterápia és a kettős terápia alkalmazása a betegek több mint 90%-ánál nem teszi lehetővé hatékony eredmény elérését. A bizmut (bizmut, tetraciklin és metronidazol) alapú triplett terápia akkor hatékony, ha a H. pylori törzs érzékeny a metronidazolra és a beteg betartja a kezelési rendet. A mellékhatások azonban gyakoriak. Az omeprazolból és 2 antimikrobiális szerből (klaritromicin és/vagy amoxicillin és/vagy metronidazol) álló triplett terápia, valamint a quadriplet terápia (bizmut alapú triplett terápia plusz omeprazol) rendkívül hatékony, és a rövidebb kúra megkönnyíti a betegek együttműködését. (1 hét). Az előzetes adatok szerint a kezelési módszer hatékonyságát nem befolyásolja az imidazollal szembeni rezisztencia.
A H. pylori eradikáció megelőzi a peptikus fekélybetegség szövődményeit és kiújulását, és költséghatékony módszer a hosszú távú savszuppressziós terápia helyett.
Ma már általánosan elfogadott, hogy a Helicobacter pylori az elsődleges kóros tényező, amely hozzájárul a gyomorhurut kialakulásához, és erősen összefügg a peptikus fekélybetegséggel. Szinte minden nyombélfekélyben szenvedő betegnél van H. pylori által kiváltott gyomorhurut. A H. pylori fertőzés és a gyomorfekély közötti kapcsolat nem sokkal kisebb, mivel a nem szteroid gyulladáscsökkentő szerek (NSAID) szedésével nem összefüggő gyomorfekélyes betegek 80%-a H. pylori-pozitív. . Mindazonáltal a H. pylori-val fertőzött egyének kisebb részében peptikus fekélybetegség alakul ki. Ebből a szempontból nyilvánvaló, hogy a törzsek variabilitásának, a makroorganizmussal kapcsolatos tényezőknek stb. is fontos szerepet kell játszaniuk a peptikus fekélybetegség patogenezisében.
A peptikus fekélybetegségben szenvedő betegek jelentős százalékánál nemcsak a gyomor-, hanem a nyombélfekélyben is szenvedő betegeknél a fekélyesedés oka az aszpirin vagy más NSAID. Az NSAID-ok és a fekélyesedés okozati összefüggése feltételezhető olyan esetekben, amikor a gyomorhurut szövettanilag nem mutatható ki a környező nyálkahártyában.
Ha azonban H. pylori-val társult gastritis lép fel, az NSAID-ok a fekélyképződés patogenezisének egyik kölcsönható tényezője lehet. A H. pylori és az NSAID-ok, mint a peptikus fekélybetegség patogenezisében leggyakrabban előforduló tényezők közötti egyértelmű kölcsönhatás nem ismert.
Bár a H. pylori fertőzés és az NSAID-ok „kényelmetlen partnerek” a peptikus fekélybetegségben, az előzetes vizsgálatok kimutatták, hogy a H. pylori eradikációja nem befolyásolja a gyógyulást vagy a visszaesést az NSAID-ekkel összefüggő peptikus fekélybetegségben. Ugyanakkor a H. pylori-pozitív betegeknél, különösen a dohányosoknál, nagyobb valószínűséggel alakul ki gyomorfekély az NSAID-kezelés során.
A H. pylori újrafelfedezése nagy hatással volt a peptikus fekélybetegség patogenezisének és kezelésének megértésére. Ez a cikk bemutatja a H. pylori felszámolásának fő irányait olyan peptikus fekélybetegségben, amely nem társul sem Zollinger-Ellison-szindrómával, sem NSAID-okkal.
1. Peptikus fekélybetegség Helicobacter pylori ellenes kezelésének javallatai
A nemzetközi munkacsoport, amely először 1990-ben Sydneyben a Gasztroenterológiai Világkongresszuson, majd 1992-ben az athéni Európai Kongresszuson ülésezett először, előzetesen kifejezte azon óhaját, hogy a H. pylori felszámolására irányuló kezelést a súlyos vagy legyengült nyombélfekélyes betegségben szenvedő betegek.
1994-ben az Országos Intézetek egészségfogalom-fejlesztéssel foglalkozó konferenciáján arra a következtetésre jutottak, hogy antimikrobiális terápiát kell előírni minden olyan betegnek, akinek dokumentált gyomorfekélye és nyombélfekélye van H. pylori fertőzéssel összefüggésben, valamint peptikus fekélybetegségben szenvedő betegek NSAID-ok szedésének hátterében, beleértve a fekély első diagnosztizálását is. Ez a vágy számos ország jelentésén alapul, amelyek meggyőzően kimutatták, hogy a H. pylori eradikációja elősegíti a fekélyek gyorsabb gyógyulását, csökkenti a kiújulási arányt és csökkenti a szövődmények arányát.
A peptikus fekélybetegség Helicobacter pylori-ellenes módszerekkel történő kezelésének megkezdése előtt az orvosnak legalább egyszer dokumentálnia kell a fekély jelenlétét. Jelenleg endoszkópiát alkalmaznak a diszpepsziás tünetek értékelésére. Ha gyomorfekélyt találnak, további szövettani vizsgálathoz biopsziát kell készíteni a rosszindulatú daganat kizárása érdekében. Az endoszkópia során nyálkahártya biopszia is elvégezhető. Ez lehetővé teszi a H. pylori fertőzés kimutatását a gyomorfekélyes betegek 90%-ának 70%-ánál és a nyombélfekélyes betegek >95%-ánál.
Főleg gyomorfekély esetén a H. pylori-t azonosítani kell, mielőtt az orvos antibiotikumos kezelést írhat elő.
Ami a nyombélfekélyt illeti, valamint azokat a betegeket, akiknek a kórelőzményében nyombélfekély szerepel, vita tárgyát képezi a H. pylori azonosításának szükségessége, mivel a valóságban 100%-os összefüggés van a mikroorganizmussal.
A nyálkahártya-biopsziák tenyésztését hagyományosan "arany standardnak" tekintik, de általában csak kutatóintézetekben használják, és a legkevésbé érzékeny diagnosztikai teszt (pozitív teszt 85-95%). Ugyanakkor előny, hogy elvégezhető az antimikrobiális érzékenységi vizsgálat. Ez nagyon hasznos lehet korábbi sikertelen irtás esetén. A H. pylori kimutatására szolgáló tenyészetminták hiányában szövettani vagy gyors ureázteszt végezhető, 90%-os szenzitivitással és 95%-os specificitással.
Ha az endoszkópiát nem végzik el, a H. pylori nem invazív módon kimutatható 13C vagy 14C jelölt karbamid kilégzési teszttel vagy szerológiai teszttel. Természetesen a pozitív teszt nem erősíti meg a peptikus fekélybetegség diagnózisát, de ezek a tesztek alkalmazhatók például olyan betegeknél, akiknek korábban dokumentált peptikus fekélybetegsége volt, és jelenleg nem észlelik a betegség tüneti megnyilvánulását. fenntartó terápia H2-hisztamin receptor blokkolókkal, ha azokat összegyűjtik a Helicobacter pylori elleni kezelés elvégzéséhez. Sajnos még nem áll rendelkezésre a H. pylori fertőzés diagnosztizálására szolgáló légzőszervi teszt, de reméljük, hogy elérhető lesz, különösen a sikeres anti-H. pylori kezelés megerősítésére.
Szerológiai tesztek is használhatók a H. pylori kimutatására. A legszélesebb körben alkalmazott módszer az enzimhez kötött immunszorbens vizsgálat (ELISA), amely költséghatékony, nagy érzékenységgel és specificitással rendelkezik. Ez a nem invazív teszt azonban csak a H. pylori fertőzést mutatja ki, és nem diagnosztizálja az aktív peptikus fekélybetegséget. Ugyanakkor a szerológiai tesztek a folyamatban lévő Helicobacter pylori elleni kezelés kontrolljaként is használhatók. Egy csepp, amely legalább 50% IgG antitestet tartalmaz titerben 3-6 hónapig, kellő pontossággal igazolhatja a H. pylori eradikációját, anélkül, hogy invazív diagnosztikai tesztekre lenne szükség.
2. H. pylori kiirtása
A H. pylori in vitro nagyon érzékeny számos antibiotikumra, bár az in vivo hatékonyság gyakran kevésbé biztató. Számos kezelési rendet alkalmaztak, amelyekben 2-4 gyógyszert kombináltak. Az egyik központ szerint nagyon hatékony kezelések nagyon gyakran hatástalanok voltak, ha más körülmények között megismételték. Néha ez magyarázható a nem kellően pontos kimutatási módszerekkel, kis mintamérettel vagy a betegek kezelési rendjének be nem tartásával. Ezen túlmenően az antibiotikumokkal, különösen a metronidazollal és valószínűleg a jövőben a klaritromicinnel szembeni rezisztencia magyarázatot adhat számos publikált tanulmány eredményeiben mutatkozó különbségekre.
Az ideális antimikrobiális szernek szűk antimikrobiális spektrumúnak kell lennie, stabilnak és aktívnak kell lennie savas pH-n (gyomor), valamint semleges pH-n (az alatta lévő régiókban és a nyálkahártya rétegében), és be kell jutnia a gyomor nyálkahártyájába is. aktív forma, behatol a nyálkahártya rétegébe akár a lumenből, akár a saját membránján keresztül. A gyógyszerek kombinációjának egyszerűnek, rendkívül hatékonynak, olcsónak és mellékhatásoktól mentesnek kell lennie, az antimikrobiális rezisztencia pedig nem növekedhet. Sajnos ilyen gyógyszerkombinációt még nem találtak, pedig a kutatók közel járnak a céljukhoz.
3. Javasolt gyógyszerkombinációk
Monoterápia
A bizmutvegyületekkel vagy antimikrobiális gyógyszerekkel végzett monoterápia nem túl hatékony. Amoxicillinnel vagy bizmutkészítményekkel végzett monoterápia esetén a H. pylori eradikációja az esetek legfeljebb 15-20%-ában érhető el.
A klaritromicin a leghatékonyabb monoterápiának bizonyult, kisszámú betegnél 15% és 54% közötti eradikációs rátával. A nitroimidazolokkal vagy makrolidokkal végzett antimikrobiális monoterápia azonban növeli a rezisztencia kialakulásának kockázatát. Ezért monoterápia nem alkalmazható a H. pylori kiirtására.
Kettős terápia
Másrészt a kettős terápia nagyon vonzó és ígéretes. A bizmutvegyületek antimikrobiális szerrel (amoxicillin, klaritromicin) való kombinációja az esetek 40-60%-ában hozzájárul a H. pylori kiirtásához. A bizmutvegyület és az imidazol (metronidazol, tinidazol) kombinációja hatásos, de nagymértékben függ az imidazollal szembeni érzékenységtől (1. táblázat).
Rövidítések: KBC - bizmut-trikálium-dicitrát (kolloid bizmut-szubcitrát); (Res.) Ќ imidazol-rezisztens, (Sen.) Ќ imidazol-érzékeny.
Goodwin et al. A H. pylori eradikációját a tinidazolra érzékeny betegek 91%-ánál sikerült elérni, de az erre a gyógyszerre rezisztens betegeknek csak 20%-ánál. Az imidazol felírása előtt meg kell határozni a beteg érzékenységét a gyógyszerre, különösen akkor, ha lokálisan magas a rezisztencia előfordulása (általában ezeknek a vegyületeknek az irracionális alkalmazása számos más fertőzés kezelésére). Franciaországban a különböző laboratóriumokban tesztelt törzsek a H. pylori nitroimidazolokkal szembeni rezisztenciájának riasztóan magas százalékát (60%) mutatták ki. Jelenleg a klaritromicinrezisztencia ritka (kevesebb, mint 5%). Bár Franciaországban, ahol a gyógyszert gyakrabban használják, az esetek 9,8% -ában rezisztenciát figyeltek meg.
A protonpumpa-gátlókról (PPI-k), például az omeprazolról amoxicillinnel vagy klaritromicinnel kombinálva beszámoltak arról, hogy elősegítik a H. pylori magas eradikációs arányát (1. táblázat). Az omeprazol-amoxicillin kombináció alkalmazásának egyik előnye, hogy az imidazollal szembeni potenciális rezisztencia irreleváns, mivel a H. pylori mindig érzékeny az amoxicillinre. Sajnos az antibiotikumok hatékonysága a dohányosoknál csökken a nemdohányzókhoz képest. Unge és munkatársai tanulmánya szerint a H. pylori kiirtását omeprazol + amoxicillin kettős kezeléssel a dohányosok mindössze 33%-ánál sikerült elérni, szemben a nemdohányzók 88%-ával.
Továbbra is tisztázatlan, hogy a PPI-k közvetlen Helicobacter-ellenes hatást fejtenek-e ki in vivo, vagy közvetetten fejtenek ki antibakteriális hatást a savtermelés erős gátlásán keresztül. Valószínű, hogy számos antibiotikum semleges pH melletti nagyobb hatékonysága magyarázza a PPI-k hatékonyságát ezekkel az antimikrobiális gyógyszerekkel kombinálva. A H. pylori kolonizációs mintázatának megváltozása az antrumból a gyomor testének zónájába, és a mikroba hajlamos arra, hogy a gyomor felszínéről a gyomorüreg mélyebb rétegeibe vándoroljon, hibákhoz vezethet elemzések, amelyek magyarázatot adnak néhány egymásnak ellentmondó irodalmi adatra a PPI és az antimikrobiális szerek kombinációjának a H. pylori eradikációjára gyakorolt hatásának hatékonyságáról ... A legtöbb vizsgálatban csak antrális biopsziát végeznek a kezelés után, így a tenyésztésből és a kórszövettani elemzésekből álnegatív eredményeket lehet kapni. Ezenkívül számos más baktérium túlszaporodása, miközben a beteget PPI-kezeléssel kezelik, hamis negatív H. pylori tenyésztési eredményekhez vezethet.
Az optimális eredmények akkor érhetők el, ha az omeprazolt naponta kétszer adják, és legalább 2 hétig antibiotikummal kombinálják, ami 24 és 93% közötti H. pylori eradikációs arányt eredményez. Ha a PPI-t az amoxicillin-kezelés megkezdése előtti héten belül alkalmazzák, a hatékonyság csökken.
Az omeprazol és a klaritromicin kombinációja is hatásos. A klaritromicin savas stabilitása és alacsony pH-oldhatósága miatt elméleti előnyökkel rendelkezik a többi makrolidhoz képest. Más makrolidoktól eltérően a gyomor nyálkahártyájában koncentrálódik, és láthatóan ez magyarázza a H. pylori eradikációjában való hatékonyságát, amely körülbelül 50%-os, még akkor is, ha monoterápiában írják fel. Az omeprazollal való kombináció jól tolerálható, és a betegek 61-72%-ánál elősegíti a H. pylori eradikációját.
A jövőben, ha a klaritromicint szélesebb körben alkalmazzák más betegségekre, rezisztencia alakul ki vele szemben, és csökken a hatékonysága.
Tripla terápia
A közzétett adatok szerint három különböző gyógyszer kombinációja bizonyult a leghatékonyabbnak. A H. pylori eradikációjának egyik leghatékonyabb sémája a bizmutsó tetraciklinnel vagy amoxicillinnel imidazolszármazékkal (metronidazollal vagy tinidazollal) kombinálva, ami körülbelül 90%-os eradikációs rátát eredményez. Ezek a sémák nagyszámú tabletta bevételét teszik szükségessé, ami megnehezíti a gondos betartásukat, emellett az eredményeket az imidazolra való érzékenység is befolyásolja (2. táblázat).
| Helicobacter pylori eradikációs ráta (hármas terápia) | |
| Kezelési rend | Az irtás mértéke |
| KBC + tetraciklin (vagy amoxicillin) + metronidazol (vagy tinidazol) | 96a* 50 (Res.), 85 (Sen.) 0 (Res.), 71 (Sen.) 50 (Res.), 98,4 (Sen.) 68 (Res.), 93 (Sen.) |
| Ranitidin + Amoxicillin + Metronidazol | 89 |
| Omeprazol + klaritromicin + tinidazol | 93,2 95 |
| Omeprazol + klaritromicin + amoxicillin | 90 |
Rövidítések: a * - imidazol érzékenységet nem vizsgáltak, de irodalmi adatok szerint nagyon alacsonynak találták a vizsgált populációban; KBC Ќ bizmut-trikálium-dicitrát (kolloid bizmut-szubcitrát); (Res.) Ќ imidazol-rezisztens, (Sen.) Ќ imidazol-érzékeny.
A triplett terápia egyik hátránya a mellékhatások magas aránya (20-50%). Általában enyhe jellegűek, és laza széklet, hányinger, fejfájás, égő érzés a szájban, bőrkiütés, szédülés vagy candidiasis. A súlyosabb mellékhatások közé tartozik a hasmenés és a pszeudomembranosus colitis.
Ugyanakkor, egy vizsgálatban 100 betegen végeztek bizmut-trikálium-dicitrátot (kolloid bizmut-szubcitrátot) napi 480 mg-os dózisban, 1000 mg tetraciklint naponta. és metronidazol 750 mg / nap. 15 napon belül kimutatták, hogy a betegek 93%-ánál sikerült a H. pylori eradikációt elérni, és csak a betegek 3%-a volt kénytelen abbahagyni a kezelést súlyos mellékhatások (súlyos hasmenés, hányinger hányással, súlyos bőrkiütés) miatt. A Gynstock által készített áttekintésben a becslések szerint a mellékhatások okozták az eradikációs terápia leállítását a betegek 8–12%-ánál.
A lehetséges mellékhatásokról szóló megfelelő tájékoztatás, az egyidejű alkohol (etanol) bevitel elkerülése és a kezelés időtartamának 2 hétre való korlátozása valószínűleg hozzájárul az ilyen típusú triplett terápia jobb toleranciájához, valamint növeli annak hatékonyságát a H. pylori felszámolásában. Az egyhetes kúra hatékonysága megegyezik a 2 hetes kúrával, de a betegek sokkal jobban tolerálják a kezelést.
Henchel és mtsai. beszámoltak arról, hogy a H. pylori 89%-ának felszámolása következik be 300 mg ranitidin 6-10 hétig tartó éjszakai, napi háromszori 750 mg amoxicillinnel és napi háromszor 500 mg metronidazollal történő kombinációja után, amelyeket először írtak fel. 10 nap. Ugyanakkor az irodalomban kevés adat áll rendelkezésre ilyen kombinációról, és az imidazollal szembeni rezisztencia jelentősen befolyásolhatja egy ilyen módszer eredményeit, ha a világ más részein alkalmazzák, ahol gyakori az ilyen rezisztencia.
Újabb, ígéretesebb és egyszerűbb technikák az omeprazol és két olyan antimikrobiális gyógyszer, mint az amoxicillin, a metronidazol és/vagy a klaritromicin alkalmazása. Ezek a kombinációk egyszerűbbek és jobban tolerálhatók, mint az eredeti „hármas” terápia.
20 mg omeprazol naponta egyszer vagy kétszer, 250 mg klaritromicin naponta kétszer és 400 mg metronidazol naponta kétszer 1 héten keresztül a H. pylori 77-88%-os felszámolását eredményezi. Ezeknek a kiváló eredményeknek a középpontjában egyértelműen a szinergia áll. Naponta kétszer 1 g amoxicillin helyettesítheti a metronidazolt ebben az új hármas adagolási rendben a hatékonyság elvesztése nélkül. Elméletileg az amoxicillint kell előnyben részesíteni, ha metronidazolrezisztencia van jelen a betegben vagy széles körben elterjedt a populációban.
Ugyanakkor a tinidazolrezisztencia hatását az omeprazol, imidazol (metronidazol vagy tinidazol) és/vagy amoxicillin és klaritromicin kombinációjával végzett kezelés kimenetelére nem vizsgálták alaposan.
Bazzoli et al. Olaszországból, ahol széles körben elterjedt az imidazol rezisztencia, a H. pylori eradikációs aránya még mindig 95% feletti volt az omeprazollal. Bell és mtsai. 2 hetes omeprazollal, amoxicillinnel és metronidazollal végzett kezelést alkalmazott. És beszámolt arról, hogy a H. pylori eradikációjának aránya 96,4% volt az imidazol-érzékeny törzsekben.
Quadriplet terápia
A Quadriplet terápia, amely bizmut, tetraciklin (vagy amoxicillin), metronidazol és PPI vegyületek kombinációja, tovább fokozza a standard triplett terápia hatékonyságát (3. táblázat). A négyes kezelés átlagosan a betegek 95%-ánál hatásos. Még a kezelés időtartamának 2 hétről 1 hétre történő csökkentése sem befolyásolta ennek a kezelési módszernek a hatékonyságát. Összehasonlítva a bizmut tartalmú triplett terápiával, a PPI hozzáadása akár 97%-kal növeli az eradikáció arányát. Korábbi jelentések azt mutatják, hogy az omeprazol hozzáadása egy még ismeretlen mechanizmus révén legyőzheti a metronidazolrezisztenciát.
| Helicobacter pylori eradikációs ráta (quadriplet terápia) | ||
| Kezelési rend | A kezelés időtartama (napokban) | Az irtás mértéke |
| KBC + tetraciklin + metronidazol + famotidin | 12 | 89a* |
| 12 | 97a* | |
| KBC + tetraciklin + metronidazol + omeprazol | 7 | 98 |
| KBC + tetraciklin + metronidazol + cimetidin (vagy ranitidin) | 7-14 | 94-95 |
| Bizmut-szalicilát + tetraciklin + metronidazol + ranitidin | 14 | 84,2 |
Rövidítések: a * - p = 0,015; NAK NEK
ВС - bizmut-trikálium-dicitrát (kolloid bizmut-szubcitrát).
Gyakorlati megközelítések és ajánlások a H. pylori fertőzés kezelésére peptikus fekélybetegségben
A H. pylori eradikációja nagymértékben javallott minden peptikus fekélybetegségben szenvedő beteg számára, mivel a fekély gyorsabb gyógyulásához vezet, csökkenti a visszaesések gyakoriságát és csökkenti a szövődmények előfordulását.
Az orvosnak számos terápiás séma áll a rendelkezésére (4. táblázat), de a gyógyszerek ideális kombinációja több tényezőtől is függ. Az anti-Helicobacter pylori terápia eredménye nagymértékben függ az imidazol/makrolidok iránti érzékenység természetétől, valamint attól, hogy a beteg megfelel-e a kezelési rendnek. Az amoxicillin a lakosság 5-10%-ánál nem alkalmazható penicillinek allergiája miatt. Előfordul, hogy a H. pylori eradikációját a beteg kezelési rendjének megfelelő betartása és a H. pylori törzs érzékenysége ellenére sem sikerül elérni, ez arra utal, hogy lehetnek más, még ismeretlen törzsek is, amelyek sikertelen eradikációhoz vezethetnek.
Rövidítések: licit - napi 2 alkalommal; tid - naponta háromszor; font - napi 4 alkalommal.
Javasoljuk a bizmut alapú triplett terápiát, bár a mellékhatások és a metronidazol-rezisztens H. pylori törzsek jelenléte jelentősen befolyásolhatja a kezelés hatékonyságát. A PPI triplet és quadriple terápia még hatékonyabb lehet, de a mellékhatások és a metronidazol-rezisztens H. pylori törzsek jelenléte a gyógyulási arányra még nem bizonyított.
Az anyagot a "Sanofi" cég ukrajnai képviselete szolgáltatja
Az ausztrál B. Marshall és R. Warren által 1982-ben felfedezett Helicobacter pylori fertőzés a gyomor és a belek különböző részeiben kialakuló fekélyek okozója. Ennek leküzdésére a nemzetközi orvosi közösség különféle eradikációs terápiás rendszereket dolgozott ki.
Veszélyes szomszéd
Jelenleg nincs kétség afelől, hogy a peptikus fekélyek nagyfokú összefüggésben állnak a Helicobacter pylori létfontosságú tevékenységével a gyomornyálkahártyában. A kezeléshez komplex eradikációs terápiát alkalmaznak - ezek a fertőzések teljes megszabadulását célzó intézkedések, amelyek minimalizálják a fekélyek megismétlődésének valószínűségét.
A H. pylori felfedezését követő években arról számoltak be, hogy ez a baktérium számos más betegség etiológiai tényezője: krónikus aktív antralis gastritis (B típus), atrófiás gastritis (A típus), nem szívrák, MALT limfóma, idiopátiás vashiányos vérszegénység, idiopátiás thrombocytopeniás purpura és B12-vitamin-hiányos vérszegénység. Folytatódik a spirál alakú baktérium allergiás, légúti és egyéb extragasztrikus betegségekkel való kapcsolatának vizsgálata.
Eradikációs terápia gyermekeknél
A gyermekek H. pylori fertőzésének felszámolásának szükségességét számos klinikai tanulmány és azok metaanalízise bizonyítja, amelyek alapul szolgáltak egy nemzetközi konszenzus dokumentum összeállításához és rendszeres frissítéséhez, amelyet a gyakorló gasztroenterológusok Maastrichti konszenzusként ismernek. Jelenleg a Helicobacter okozta betegségek diagnosztizálásának és kezelésének kérdéseit a 2010-ben elfogadott negyedik maastrichti konszenzus szabályozza.
Európa, Amerika és Ausztrália fejlett országaiban, ahol a H. pylori etiológiai szerepének felfedezése óta szisztematikusan fejlesztették ki és vezették be a gyakorlatba a fertőzés diagnosztizálására és kezelésére szolgáló módszereket, csökkent a peptikus fekély előfordulása. és krónikus gyomorhurutot észleltek. Ráadásul ezekben az országokban évtizedek óta először megfigyelhető a gyomorrák incidenciájának csökkenése, amit az eradikációs terápia is elősegít.

Titokzatos baktériumok
Számos randomizált placebo és összehasonlító vizsgálat eredményei alapján meghatározták a probiotikus szerek hatékonyságát különböző klinikai helyzetekben, beleértve a Helicobacter pylori fertőzést gyermekeknél. A probiotikumok H. pylori baktériumra gyakorolt hatásának megértésében elért előrelépések ellenére azonban finom mechanizmusai továbbra is kevéssé ismertek.
A Lactobacillusok fő gátló és baktériumölő faktora a tejsav, amelyet nagy mennyiségben termelnek. A tejsav gátolja a H. pylori ureáz aktivitását, és vélhetően úgy fejti ki antimikrobiális hatását, hogy csökkenti a pH-t a gyomor lumenális terében. Azt találták azonban, hogy a tejsav, amelyet a gyomornyálkahártya (GSS) sejtjei termelnek, elősegíti a H. pylori telep növekedését. A tejsav mellett a laktobacillusok és néhány más probiotikus törzs is termel antibakteriális peptideket.
Komplex terápia
Az eradikációs terápia koncepciója a gyógyszerek kombinációján alapul. A PPI-k (protonpumpa-gátlók) gátolják az ureáz enzim működését és az energia felhalmozódását a H. pyloriban, valamint emelik a gyomornyálkahártya pH-ját, megteremtve az antibakteriális gyógyszerek hatásának feltételeit. A baktériumokban felhalmozódó bizmutsók megzavarják a kórokozó enzimrendszerét, így a gyermek immunrendszere hatékonyabban tud megbirkózni a „megszállóval”. Végül a legváltozatosabb csoport az antibakteriális gyógyszerek csoportja.
A gyermekek peptikus fekélybetegségének eradikációs terápiája (mint a gyomorhurut esetén) gyakran nitroimidazolok, makrolidok, laktámok, tetraciklin és nitrofuránok alkalmazását foglalja magában. A Helicobacter rezisztenciát fejleszt ki az antibakteriális komponensekkel szemben, ami csökkenti az eradikációs terápia hatékonyságát. És ennek a problémának a sürgőssége minden évtizedben növekszik.

Antibiotikum rezisztencia
Az antibiotikum-rezisztencia kialakulása minden kórokozó mikroorganizmusra jellemző. Ez egy evolúciós mechanizmus, amely biztosítja a túlélésüket a változó körülmények között. A H. pylori rezisztencia a következőkre oszlik:
- Elsődleges (a korábbi kezelés következménye).
- Másodlagos (a mikroorganizmus szerzett mutációja, amelyet az eradikációs terápia "ösztönöz").
A kezelésrezisztencia okai
A tudósok megnevezik a H. pylori szerzett rezisztencia kialakulásának fő okait:
- Az azonos csoportba tartozó antibakteriális gyógyszerek felírásának növekedése más indikációkra.
- Ellenőrizetlen öngyógyítás antibiotikumokkal azokban az országokban, ahol vény nélkül árusítják őket.
- Nem megfelelően előírt eradikációs terápia gyomorhurut vagy fekély esetén (kis dózisú antibiotikum felírása, a kezelés lerövidítése, helytelen kombináció a gyógyszeres kezelésben).
- Az orvos előírásainak be nem tartása a betegek részéről.
- Alacsony minőségű gyógyszerek megjelenése a gyógyszerpiacon.
A fentiek eredményeként a H. pylori rezisztencia növekedése csökkenti az e mikroorganizmus ellen aktív antibiotikumok amúgy is korlátozott számát.
Az antibiotikum-rezisztencia problémája különösen fontos azoknál a gyermekeknél, akiknél peptikus fekélybetegség esetén eradikációs terápiát kapnak. Leggyakrabban a szülőktől és közeli rokonoktól származó, elsősorban rezisztens mikroorganizmusokkal fertőződnek meg.
Emellett a gyermekpopulációban különösen elterjedt az antibiotikumok indokolatlan alkalmazása egyéb betegségek, leggyakrabban légúti fertőzések kezelésére, ami szintén hozzájárul az elsősorban rezisztens törzsek kiválasztásához. Az eradikációs terápia rendjének megsértése, mint a felnőtteknél, másodlagos rezisztencia kialakulásához vezet. A patogén rezisztencia kialakulása a Helicobacter pylori különböző génjeinek mutációival is összefügg.

Diagnosztika
A serdülők eradikációs terápiája átfogó diagnózis után kezdődik. A gyomor-bélrendszeri tünetekkel küzdő gyermek értékelésének elsődleges célja a tünetek okának meghatározása, nem csak a H. pylori jelenlétének meghatározása. Ugyanakkor a Helicobacter kimutatására szolgáló tesztek nem javasoltak funkcionális hasi fájdalomban szenvedő gyermekeknél. Megfontolhatja a kórokozó azonosítására szolgáló vizsgálatok elvégzésének megvalósíthatóságát:
- olyan betegeknél, akiknek a családjában előfordult gyomorrák első fokú rokonánál;
- refrakter vashiányos vérszegénység esetén (ha a betegség egyéb okait kizárják).
Nincs elegendő gyakorlati bizonyíték a H. pylori szerepére középfülgyulladásban, felső légúti fertőzésekben, parodontitiszben, ételallergiában, hirtelen csecsemőhalál szindrómában, idiopátiás thrombocytopeniás purpurában és alacsony termetben. De vannak gyanúk.
Diagnosztikai vizsgálatok
A peptikus fekély és gyomorhurut eradikációs terápiáját diagnosztikai tesztek határozzák meg. A vizsgálati módszer számos tényezőtől függ:
- A Helicobacter oesophagogastroduodenoscopia során történő diagnosztizálásához javasolt a gyomor antrumának biopsziája további szövettani elemzés céljából.
- Javasoljuk, hogy a H. pylori kezdeti diagnózisa a következő eredményeken alapuljon: pozitív szövettani vizsgálat és pozitív ureáz teszt (vagy pozitív tenyésztési eredmények).
- A C-ureáz kilégzési teszt megbízható, nem invazív módszer annak meghatározására, hogy a H. pylori-t kiirtották-e.
- A széklet immunszorbens vizsgálata szintén megbízható, nem invazív teszt annak meghatározására, hogy a baktériumokat kiirtották-e.
- Éppen ellenkezőleg, a Helicobacter elleni antitestek szérumban, teljes vérben, vizeletben és nyálban történő kimutatásán alapuló tesztek nem megbízhatóak.

Javallatok
Mik az eradikációs terápia javallatai:
- Peptikus fekély és Helicobacter fertőzés jelenlétében.
- Ha nincs peptikus fekélybetegség, és a biopsziával vett minták vizsgálatának eredménye alapján H. pylori fertőzést azonosítottak, a kórokozó felszámolása opcionális, de lehetséges.
Járványtan
Az ellenállás szintjének meghatározása egy adott országban, régióban vagy népességben nehéz feladat, amely nagy anyagi és emberi erőforrásokat igényel. A különböző országokból származó adatok összehasonlítása a kutatási módszertani különbségek miatt még nehezebb. Például az Európában (2003-2011) végzett hosszú távú vizsgálatok anyagai szerint a kórokozó Clarithromycinnel szembeni rezisztenciája a különböző országokban 2-64% között mozgott. Orosz szerzők szerint a klaritromicinnel szembeni rezisztencia 5,3 és 39% között változik.
A felszámolási sémákban használt gyógyszerek közül a legkisebb rezisztenciát az amoxicillin, a legnagyobb pedig a "metronidazol" okozza. A H. pylori klaritromicinnel szembeni rezisztenciája tovább növekszik.
A "Metronidazol" és a "Furazolidone" használatának problémái
Az eradikációs terápiát gyakran a fenti gyógyszerekkel végezték. Azonban a baktériumok növekedése a Metronidazolhoz való alkalmazkodóképessége élesen csökkentette a kezelési rendek hatékonyságát a használatával. Emiatt a "Metronidazol" számos országban ki van zárva a kezelési rendekből.
A metronidazol alternatívája a nitrofurán készítmények, különösen a furazolidon. Az irtási hatékonyság az alapján bizmuttal kombinálva 86%. A "Furazolidone" azonban mérgező - sok klinikán nem használják gyermekgyógyászati terápiában. A "Furazolidone" hátrányai közé tartozik a hepato-, neuro- és hematotoxicitás, a mikroflóra elnyomása, a nem kielégítő organoleptikus tulajdonságok. A hatóanyag szükséges koncentrációjának eléréséhez a szervezetben ezt a gyógyszert naponta négyszer kell bevenni. A "Furazolidone" ezen tulajdonságai jelentősen csökkentik a teljes kezelési rend jótékony hatását, és ennek következtében az irtás hatékonyságát.

Új generációs gyógyszer
A gyógyszergyárak számos laboratóriuma fejleszt olyan gyógyszereket, amelyek kevésbé mérgezőek, de hatékonyak a Helicobacter ellen. Igazi áttörést jelentett a "Macmiror" gyógyszer, amely hatóanyagként nifuratelt tartalmazott. A "Furazolidone" modern alternatíváját a Polichem (Olaszország) kutatócég fejlesztette ki és szintetizálta. A "Macmiror" antibakteriális, gombaellenes és protozoális hatás széles spektrummal rendelkezik. A gyermekek kiirtási terápiája biztonságosabbá vált.
A "Makmirora" használata lehetővé teszi a Helicobacter gyermekeknél történő felszámolására vonatkozó meglévő rendszerek javítását, hatékonyságuk és biztonságuk növelését. A "Nifuratel" szerepel a H. pylori-val összefüggő krónikus gastritis, gastroduodenitis és peptikus fekélybetegség kezelésére szolgáló frissített protokollokban gyermekeknél.
A "Macmiror" gyógyszer alkalmazása magas megfeleléssel jár, mivel a tizenkét órás felezési idő miatt naponta kétszer írható fel. Hat éves kortól gyermekeknél alkalmazzák, a napi adag a giardiasis kezelésében és a Helicobacter felszámolásában napi 30 mg a gyermek súlyának kilogrammonként.
Irtásterápiás sémák
Példák az első vonalbeli terápiára. Egyhetes hármas kúrák bizmut készítménnyel:
- A kolloid bizmut-szubcitrátot (BSC) amoxicillinnel (Roxithromycin) vagy Clarithromycinnel (Azithromycin) és Nifuratel-lel (Furazolidon) egészítik ki.
- A második sémában a "Nifuratel" helyébe "Famotidin" ("Ranitidin") lép, a többi gyógyszer ugyanaz.
Egyhetes hármas kezelések protonpumpa-gátlókkal:
- Az omeprazolt (Pantoprazolt) amoxicillinnel vagy klaritromicinnel és Nifuratel-lel (Furazolidon) egészítik ki.
- Ugyanaz, de a "Nifuratel" helyett SWR.
Második vonalbeli kezelésként a négy komponensből álló eradikációs terápiát alkalmazzák: a KSV együtt működik az omeprazollal (Pantoprazol), az amoxicillinnel (vagy klaritromicinnel) és a nifuratellel (furazolidon).

Dózisok
A protokollok szabályozzák a gyermekek eradikációs kezelésében alkalmazandó gyógyszerek adagját is (naponta testtömeg-kilogrammonként):
- KSV - 48 mg (maximum 480 mg naponta).
- Klaritromicin - 7,5 mg (maximum 500 mg).
- "Amoxicillin" - 25 mg (maximum 1 g).
- Roxitromicin - 10 mg (maximum 1 g).
- "Furazolidon" - 10 mg.
- "Nifuratel" - 15 mg.
- Omeprazol - 0,5-0,8 mg (maximum 40 mg).
- "Pantoprazol" - 20-40 mg (súly nélkül).
- "Ranitidin" - 2-8 mg (maximum 300 mg).
- Famotidin - 1-2 mg (maximum 40 mg).
A kezelés jellemzői
Milyen kezelést kell alkalmazni egy adott helyzetben:
- Azok a gyermekek, akik H. pylori-val fertőzöttek, és a családban előfordult gyomorrák első fokú rokonánál, eradikációs terápiát kaphatnak.
- Javasoljuk az antibiotikum-rezisztens Helicobacter törzsek előfordulásának nyomon követését a különböző régiókban.
- Azokban a régiókban/populációkban, ahol a Helicobacter klaritromicinnel szembeni rezisztenciája magas (> 20%), a klaritromicin hármas terápia megkezdése előtt ajánlott meghatározni az antibiotikum érzékenységét.
- A hármas terápia javasolt időtartama 7-14 nap. Ennek a kérdésnek a mérlegelésekor figyelembe kell venni a költségeket, a betartást és a mellékhatásokat.
- Az elvégzett eradikációs terápia eredményeinek értékeléséhez a kezelés után 4-8 héttel megbízható non-invazív tesztek alkalmazása javasolt.
Ha nem segít
- Esophagogastroduodenoscopy, majd tenyésztés és antibiotikum-érzékenységi vizsgálat, beleértve az alternatív vizsgálatokat is, ha nem végezték el a kezelés előtt.
- Fluoreszcencia in situ hibridizáció (FISH) a "Clarithromycin"-rel szembeni rezisztencia meghatározására az első biopsziánál vett és paraffinba ágyazott minták felhasználásával, ha az antibiotikumra való érzékenység meghatározását a kezelés előtt nem végezték el.
- A kezelés módosítása: adjon hozzá egy antibiotikumot, írjon fel másik antibiotikumot, adjon hozzá bizmutot és/vagy növelje az adagot, és/vagy hosszabbítsa meg a terápia időtartamát.
Következtetés
Az eradikációs terápia hatékony (néha az egyetlen) eszköz a legveszélyesebb Helicobacter pylori baktérium elleni küzdelemben, amely fekélyt, gyomorhurutot, vastagbélgyulladást és más gyomor-bélrendszeri betegségeket okozhat.
Helicobacter pylori(lat. ) egy spirális Gram-negatív mikroaerofil baktérium, amely megfertőzi a gyomor és a nyombél nyálkahártyáját. Néha hívják Helicobacter pylori(lásd Zimmerman Y.S.).
Helicobacter pylori tévhitek
Gyakran észleléskor , a betegek aggódni kezdenek azok felszámolása (megsemmisítése) miatt. Maga a rendelkezésre állás a gyomor-bél traktusban nem indokolja az azonnali antibiotikum- vagy más szeres kezelést. Oroszországban a felszólalók száma eléri a lakosság 70%-át, és túlnyomó többségük nem szenved semmilyen gyomor-bélrendszeri betegségben. A felszámolási eljárás két antibiotikum (például klaritromicin és amoxicillin) bevételéből áll. Az antibiotikumokra fokozott érzékenységű betegeknél allergiás reakciók lehetségesek - az antibiotikumokkal összefüggő hasmenéstől (nem súlyos betegség) a pszeudomembranosus colitisig, amelynek valószínűsége kicsi, de a halálozási arány magas. Ezenkívül az antibiotikumok szedése negatívan befolyásolja a belek, a húgyutak "barátságos" mikroflóráját, és hozzájárul az ilyen típusú antibiotikumokkal szembeni rezisztencia kialakulásához. Bizonyíték van arra, hogy a sikeres felszámolás után a következő néhány évben a gyomornyálkahártya újrafertőződése a leggyakrabban megfigyelhető, amely 3 év után 32 ± 11%, 5 év után 82–87%, 7 év után pedig 90,9% (Zimmerman Y.S.).Amíg a fájdalom meg nem nyilvánul, a helikobakteriózist nem szabad kezelni. Sőt, nyolc év alatti gyermekeknél általában nem javasolt eróziós kezelést végezni, mivel immunitásuk még nem alakult ki, antitestek nem keletkeznek. Ha 8 éves koruk előtt végzik az irtást, akkor egy nap múlva, miután rövid beszélgetést folytattak más gyerekekkel, "megragadják" ezeket a baktériumokat (PL Shcherbakov).
Felszámolás ajánlható a gyomorrák kockázatának csökkentésére. Ismeretes, hogy az eperákos esetek legalább 90%-a H. pylori fertőzéssel (Starostin B.D.) kapcsolódik.
 |
 |
 |
| kísérletileg monofertőzött egerekből (A), humán gyomornyálkahártyából (B) és agarlemezen tenyésztettük (C). Mindkettőt kísérletileg fertőzött egerekből és humán biopsziából izolálták durva, és a flagellák hajlamosak összetapadni. A coccoid forma kivételével a morfológia viszonylag jól megőrződött az agartenyészetben (C). Skálajelek = 1 μm. Forrás: Stoffel M.H. et al. A gyomor Helicobacter spp. in Humans and Domestic Pets by Scanning Electron Microscopy / 2001. január. DOI: 10.1046 / j.1523-5378.2000.00036.x. Blackwell Science, 1083-4389 / 00 / 232-239. Inc. 5. évfolyam 4. szám 2000. | ||
Helicobacter pylori virulencia faktorok
Számos virulenciafaktor ismert, amelyek lehetővé teszik benépesül, majd megmarad a gazdaszervezetben (Skvortsov V.V., Skvortsova E.M.).- Flagella megengedi gyomornedvben és nyálkarétegben mozog.
- képes a gyomorhámsejtek plazmolemmájához kapcsolódni, és elpusztítani e sejtek citoszkeletonjának összetevőit.
- ureázt és katalázt termel. Az ureáz lebontja a gyomornedvben lévő karbamidot, ami növeli a mikroba közvetlen környezetének pH-értékét és megvédi a gyomor savas környezetének baktériumölő hatásától.
- képes elnyomni bizonyos immunválaszokat, különösen a fagocitózist.
- adhezineket termel, amelyek elősegítik a baktériumok adhézióját a hámsejtekhez, és gátolják fagocitózisukat a polimorfonukleáris leukociták által.
Helicobacter pylori okozta nyombélfekély
Fő élőhely a gyomor antrumának nyálkahártyája, amelyet a gyulladásos és atrófiás folyamat érint - a gyomorhuruthoz társuló ... A nyombélfekély kialakulásához kapcsolódó , szükséges a gyomor metaplázia jelenléte a duodenum nyálkahártyájában, ami viszont a duodenum savasságának növekedésével jár. Így a nyombélfekély társul és a duodenitis mindig a duodenumban jelentkező savas-peptikus agresszió hátterében alakul ki, i.e. ugyanakkor savfüggő patológiák is. Ebben az esetben a sósav gyomorban történő hiperszekréciójának legfontosabb tényezője a közvetlen hatás a szekréciós folyamatra a gyomor antrumának túlzott lúgosításával az ureáz által termelt karbamid hidrolízis termékeivel ... A túlzás következménye a lúgosodás hipergasztrinaemia, ami viszont a sósav túltermeléséhez vezet. A savtermelés szabályozásának zavarai betegeknél, amelyekhez társul A gastritist a fertőzésre válaszul az antrum nyálkahártyájában szintetizáló specifikus gyulladásos folyamat és mediátorai (citokinek és epidermális növekedési faktorok) is okozzák. , különösen kifejezett a citotoxikus törzsekben. Ezek a törzsek nem csak súlyos gyulladást okozhatnak a gyomorban, hanem hozzájárulnak a destruktív folyamatok kialakulásához - fekélyek kialakulásához, beleértve a duodenumban a gyomor metaplasia területein. Ezt elősegítik a duodenális környezet agresszív tényezői, a nyálkahártya-gát védő tulajdonságainak csökkenése, a károsodott mikrokeringés (beleértve a ), örökletes hajlam. Mindezek a folyamatok fekélyek megjelenéséhez vezetnek (Maev I.V., Samsonov A.A.).
a lúgosodás hipergasztrinaemia, ami viszont a sósav túltermeléséhez vezet. A savtermelés szabályozásának zavarai betegeknél, amelyekhez társul A gastritist a fertőzésre válaszul az antrum nyálkahártyájában szintetizáló specifikus gyulladásos folyamat és mediátorai (citokinek és epidermális növekedési faktorok) is okozzák. , különösen kifejezett a citotoxikus törzsekben. Ezek a törzsek nem csak súlyos gyulladást okozhatnak a gyomorban, hanem hozzájárulnak a destruktív folyamatok kialakulásához - fekélyek kialakulásához, beleértve a duodenumban a gyomor metaplasia területein. Ezt elősegítik a duodenális környezet agresszív tényezői, a nyálkahártya-gát védő tulajdonságainak csökkenése, a károsodott mikrokeringés (beleértve a ), örökletes hajlam. Mindezek a folyamatok fekélyek megjelenéséhez vezetnek (Maev I.V., Samsonov A.A.). Helicobacter pylori felszámolási rendek
Az Egészségügyi Világszervezet aktív gyógyszerekkel kapcsolatban beleértve a metronidazolt, tinidazolt, kolloid bizmut-szubcitrátot, klaritromicint, amoxicillint és tetraciklint (Podgorbunskikh E.I., Maev I.V., Isakov V.A.).
Felszámolás nem mindig éri el a célt. Az elterjedt antibakteriális szerek nagyon széles körben elterjedt és nem megfelelő használata azokkal szembeni fokozott rezisztenciához vezetett. ... A jobb oldali ábra (Belousova Yu.B., Karpov O.I., Belousov D.Yu. és Beketov A.S. cikkéből vett) a törzsek metronidazollal, klaritromicinnel és amoxicillinnel szembeni rezisztenciájának dinamikáját mutatja. elkülönítve a felnőttektől (fent) és a gyerekektől (lent). Elismert tény, hogy a világ különböző országaiban (különböző régiókban) különböző sémákat célszerű alkalmazni. Az irtásra vonatkozó ajánlásokat az alábbiakban közöljük. Az oroszországi Gasztroenterológusok Tudományos Társasága által 2010-ben elfogadott, a savfüggő és Helicobacter pylori-val összefüggő betegségek diagnosztizálására és kezelésére vonatkozó szabványokban meghatározott szabványok. A felszámolási eljárás megválasztása attól függ, hogy a betegek egyéni intoleranciát mutatnak-e bizonyos gyógyszerekre. , valamint a törzsek érzékenysége ezekre a gyógyszerekre. A klaritromicin eradikációs rendszerben történő alkalmazása csak olyan régiókban lehetséges, ahol a vele szembeni rezisztencia 15-20% alatti. 20% feletti ellenállású régiókban csak az érzékenység meghatározása után célszerű használni klaritromicinre bakteriológiai módszerrel vagy polimeráz láncreakcióval.

Oroszországban nincsenek teljes körű tanulmányok a klaritromicin-rezisztens törzsek prevalenciájáról H. pylori... Vannak azonban olyan helyi tanulmányok, amelyek mindegyikében a Maastricht IV terminológiájában alacsony ellenállási szintet állapítottak meg, és ez alapján orosz körülmények között nagy valószínűséggel célszerűbb a séma bal oldalát használni. , zölddel jelölve.
Szakmai orvosi publikációk a Helicobacter pylori-val kapcsolatos betegségekről
- Ivashkin V.T., Maev I.V., Lapina T.L. és az Orosz Gasztroenterológiai Szövetség egyéb klinikai irányelvei a Helicobacter pylori fertőzés diagnosztizálására és kezelésére felnőtteknél // RZHGGK. 2018. 28. szám (1). S. 55–77.
- Ivaskin V.T., Maev I.V., Lapina T.L., Sheptulin A.A., Trukhmanov A.S., Abdulhakov R.A. et al. A Helicobacter pylori fertőzés kezelése: mainstream és innováció // Ros Zhurn gastroenterol hepatol coloproctol. 2017. 27. szám (4). S. 4-21.
- A savfüggő és a Helicobacter pylori okozta betegségek diagnosztizálásának és kezelésének szabványai (az ötödik moszkvai megállapodás) // A NOGR XIII. Kongresszusa. 2013. március 12
- A savfüggő és a Helicobacter pylori-val összefüggő betegségek diagnosztizálására és kezelésére vonatkozó szabványok (a negyedik moszkvai megállapodás) / Moszkva Város Egészségügyi Osztályának 37. sz. irányelvei. - M .: TsNIIG, 2010 .-- 12 p.
- Zimmerman Ya. S. Peptikus fekély: a probléma jelenlegi állapotának kritikai elemzése // Kísérleti és klinikai gasztroenterológia. - 2018 .-- 149 (1). S. 80–89.
- E. A. Kornienko, N. I. Parolova A Helicobacter pylori antibiotikum-rezisztenciája gyermekeknél és a terápia megválasztása // A modern gyermekgyógyászat kérdései. - 2006. - 5. évfolyam - 5. szám - p. 46-50.
- Zimmerman Ya.S. A mikroorganizmusok antibakteriális terápiával szembeni növekvő rezisztenciájának problémája és a Helicobacter pylori fertőzés felszámolásának kilátásai / A könyvben: A modern gasztroenterológia megoldatlan és vitatott problémái. - M .: MEDpress-inform, 2013.S. 147-166.
- A Helicobacter pylori fertőzés diagnosztikája és kezelése - a Maastricht IV / Firenzei egyeztető konferencia beszámolója // Egy gyakorlati orvos értesítője. Különszám, 2012. 1., 6-22.
- Isakov V.A. A Helicobacter pylori fertőzés diagnosztizálása és kezelése: IV Maastrichti Megállapodás / Új irányelvek a H. pylori fertőzés diagnosztizálásához és kezeléséhez - Maastricht IV (Firenze). A legjobb klinikai gyakorlat. orosz kiadás. 2012. 2. szám. S.4-23.
- Maev I.V., Samsonov A.A., Andreev D.N., Kochetov S.A., Andreev N.G., Dicheva D.T. A Helicobacter pylori fertőzés diagnózisának és kezelésének modern szempontjai // Orvosi Tanács. 2012. 8. sz. C. 10-19.
- Rakitin B.V. Tájékoztató a Helicobacter pylori fertőzés "Maastricht V" diagnosztizálásáról és kezeléséről szóló egyeztető konferenciáról Lei M. beszámolójából a Központi Földtani Tudományos Kutatóintézet 42. tudományos ülésszakán, 2016. március 2-3.
- Maev I.V., Rapoport S.I., Grechushnikov V.B., Samsonov A.A., Sakovich L.V., Afonin B.V., Aivazova R.A. A légzéstesztek diagnosztikai értéke a Helicobacter pylori fertőzés diagnosztizálásában // Klinikai gyógyászat. 2013. 2. szám P. 29–33.
- Kazyulin A.N., Partsvania-Vinogradova E.V., Dicheva D.T. és egyéb Az anti-Helicobacter pylori terápia optimalizálása a modern klinikai gyakorlatban // Consilium medicum. - 2016. - 8. sz. - 18. évfolyam 32-36.
- Malfertheiner P, Megraud F, Morain CAO, Gisbert JP, Kuipers EJ, Axon AT, Bazzoli F, Gasbarrini A et al. A Helicobacter pylori fertőzés kezelése – a Maastricht V / Florence Consensus Report // Gut 2016; 0: 1–25. doi: 10.1136 / gutjnl-2016-312288.
- B. D. Starostin Helicobacter rulo fertőzés kezelése - Maastricht V / Firenzei konszenzus jelentés (megjegyzésekkel lefordítva) // Szentpétervári gasztroenterológia. 2017; (1): 2-22.
- Maev I.V., Andreev D.N., Dicheva D.T. és egyéb A Helicobacter pillory fertőzés diagnosztikája és kezelése. Konszenzusos rendelkezések Maastricht V (2015) // Archives of Internal Medicine. Klinikai irányelvek. - 2. szám - 2017. S. 85-94.
- Oganezova I.A., Avalueva E.B. Helicobacter pylori-negatív peptikus fekélybetegség: történelmi tények és modern valóság. Pharmateca. 2017; Gasztroenterológia / Hepatológia: 16-20.
A Helicobacter pylori felszámolása terhes és szoptató anyáknál
Felszámolás Helicobacter pylori a Maastrichti Konszenzus II-2000 és III-2005 szerint terhes nőkön nem végzik el. Az irtás kérdésének megoldása Helicobacter pylori a szülés és a szoptatási időszak vége után helyezték el (Rebrov B.A., Komarova E.B.).A Helicobacter pylori előfordulása különböző országokban és Oroszországban
A Gasztroenterológiai Világszervezet szerint ( fejlődő országokban, 2010, WGO) a világ lakosságának több mint fele hordozó ), míg a fertőzés előfordulása jelentősen eltér az egyes országokban, valamint ezeken az országokon belül. Általában a fertőzés az életkorral növekszik. A fejlődő országokban fertőzés sokkal hangsúlyosabb a fiataloknál, mint a fejlett országokban. A VGO a következő számokat adja:
| Ország (régió) | Korcsoportok | Fertőzési arány |
| Európa | ||
| Kelet-Európa | felnőttek | 70 % |
| Nyugat-Európa | felnőttek | 30-50 % |
| Albánia | 16-64 | 70,7 % |
| Bulgária | 1-17 | 61,7 % |
| cseh | 5-100 | 42,1 % |
| Észtország | 25-50 | 69 % |
| Németország | 50-74 | 48,8 % |
| Izland | 25-50 | 36 % |
| Hollandia | 2-4 | 1,2 % |
| Szerbia | 7-18 | 36,4 % |
| Svédország | 25-50 | 11 % |
|
Észak Amerika |
||
| Kanada | 5-18 | 7,1 % |
| Kanada | 50-80 | 23,1 % |
| USA és Kanada | felnőttek | 30 % |
|
Ázsia |
||
| Szibéria | 5 | 30 % |
| Szibéria | 15-20 | 63 % |
| Szibéria | felnőttek | 85 % |
| Banglades | felnőttek | > 90 % |
| India | 0-4 | 22 % |
| India | 10-19 | 87 % |
| India | felnőttek | 88 % |
| Japán | felnőttek | 55-70 % |
|
Ausztrália és Óceánia |
||
| Ausztrália | felnőttek | 20 % |
A populációk közötti társadalmi-gazdasági különbségek felelősek lehetnek az eltérő fertőzési arányért. Fertőzés főként orális-orális vagy széklet-orális úton fordul elő. A higiénia, a biztonságos ivóvíz, az alapvető higiéniai elvek hiánya, valamint a korlátozott táplálkozás és a nagyszámú populáció szerepet játszhat a fertőzések magas prevalenciájában.
Oroszország azon országok közé tartozik, ahol nagyon magas a H. pylori fertőzés előfordulása. Egyes régiókban, például Kelet-Szibériában, ez a szám meghaladja a 90%-ot mind a mongoloid, mind a kaukázusi populációban. Moszkvában fertőzés lent. A Központi Gasztroenterológiai Kutatóintézet szerint Moszkva keleti közigazgatási körzetének lakosságának körülbelül 60% -a Helicobacter hordozó. Bár a lakosság bizonyos csoportjaiban a Helicobacter gyakoribb. Különösen a moszkvai ipari vállalkozások dolgozói fertőzöttek 88 % (
A Helicobacter pylori egy olyan baktérium, amely a nyombél és a gyomor betegségeinek kórokozójává válhat. A fekélyek, gyomorhurut, nyombélgyulladás és még rákos daganatok is gyakran ennek a mikroorganizmusnak az elterjedésének az eredménye. A baktériumok speciális szerkezetének köszönhetően behatolhat a nyálkahártyába, és ott nyugodtan telepeket hozhat létre.
A Helicobacter pylori-val kapcsolatos betegségek kezelésekor fontos, hogy intézkedéseket hozzanak a baktériumok teljes megsemmisítésére. Csak akkor tekinthető hatékonynak, ha a gyógyulás valószínűsége megközelíti a 80%-ot. Az ilyen kezelés átlagos időtartama körülbelül két hét, és a mellékhatások valószínűsége nem haladhatja meg a 15% -ot. Legtöbbjük nem súlyos, vagyis miattuk nem szükséges megszakítani a gasztroenterológus által felírt gyógyszerek kezelését.
Kezelési rendek
A terápiás sémának mindenekelőtt állandó magas szintű baktériummentesítést kell biztosítania. A Helicobacter pylori felszámolásának sémáját egyedileg választják ki, a baktériumok érzékenységétől és a szervezet gyógyszerre adott válaszától függően.
Számos felszámolási (felszámolási) program létezik, és ezek száma idővel növekszik. Ezen túlmenően mindegyik számos feladat megvalósítására irányul, beleértve a következőket:
Sémák kidolgozása
Jelen pillanatban a fenti területek mindegyikén jelentős eredmények születtek a tudósok és a gyógyszergyárak együttműködésének köszönhetően. A múlt század végén megalakult az ipar legbefolyásosabb szakembereiből egy csoport, amelynek erőfeszítései az irtással kapcsolatos ismeretek megosztására irányulnak.
Ez áttörést tett lehetővé a kezelések fejlesztése és a hatékonyabb vizsgálatok terén. A legnagyobb előrelépés az 1996-os maastrichti konferencián történt. Ennek az eseménynek a tiszteletére később a Helicobacter pylori kezelésére szolgáló komplexeket nevezték el.
- amoxicillin (0,5 g naponta négyszer vagy 1 g - 2 alkalommal);
- klaritromicin vagy josamicin vagy nifuratel (standard dózisok);
- bizmut-trikálium-dicitrát (240 mg naponta kétszer vagy a dózis fele - négyszer).
A fenti sémát csak a gyomornyálkahártya atrófiájában szenvedő betegeknél alkalmazzák.
A negyedik lehetőség (idős betegek számára):
- az inhibitorok standard dózisa;
- bizmut-trikálium-dicitrát;
A negyedik lehetőség (alternatíva) a bizmut-trikálium-dicitrát szokásos adagokban történő bevétele 28 napig, gátlószerek esetleges rövid távú alkalmazásával.
Második sor
Látható hatás hiányában az irtás második vonalát alkalmazzák, amely lehetővé teszi az eljárás hatékonyságának növelését.
Első lehetőség:

Második lehetőség:
- inhibitorok;
- bizmut-trikálium-dicitrát;
- a nitrofurán csoport készítményei;
Harmadik lehetőség:
- protonpumpa-gátló;
- bizmut-trikálium-dicitrát (csak 120 mg naponta négyszer);
- rifaximin (0,4 g naponta kétszer).
Harmadik sor
Létezik egy harmadik vonal is, de ennek elterjedése a fent felsorolt lehetőségek nagy hatékonysága miatt minimális. Ez a séma csak olyan esetekben alkalmazható, amikor az indikációk nem teszik lehetővé az első kettő alkalmazását allergiás reakciók vagy nem kielégítő kezelési reakció miatt.
A szisztematikus áttekintés és metaanalízis eredményei
A H. pylori fertőzés a gyomor- és nyombélfekély, a gyomor MALT limfómák és a gyomorrák okozója. Jelenleg számos eradikációs terápiás sémát javasoltak: standard hármas terápia amoxicillinnel, klaritromicinnel és protonpumpa-gátlóval (PPI); bizmutkészítményeken alapuló kvadroterápia, szekvenciális és egyidejű terápia. Az egyik jelenlegi globális kihívás a klaritromicinnel és a metronidazollal szembeni növekvő rezisztencia. A probléma leküzdésére a klinikai gyakorlatban egyre gyakrabban kezdték el alkalmazni a szekvenciális terápiát, beleértve a PPI és az amoxicillin kijelölését naponta kétszer 1 g adagban az első öt napban, valamint PPI-t, 500 mg klaritromicint kétszer. egy nap és egy gyógyszer a nitromidazolok csoportjából 500 mg-os dózisban naponta kétszer. A közelmúltban végzett tanulmányok, amelyek ezt a kezelési rendet a hármas terápiával hasonlították össze, biztató eredményekkel szolgálnak, és az új eradikációs rendszer hatékonyságára utalnak.
Cél
Hasonlítsa össze a szekvenciális eradikációs terápiát a H. pylori fertőzés más eradikációs kezelési rendjeivel.
Anyagok és metódusok
A tanulmány olyan randomizált kontrollált vizsgálatokat (RCT) tartalmazott, amelyeket olyan adatbázisokban kerestek, mint a Medline (1950-től 2013 májusáig), az Embase-en (1980-tól 2013 májusáig) és a Cochrane Central Register of Controlled Trials-en (2013 májusáig). A szekvenciális terápiát összehasonlították másokkal. eradikációs sémák 18 év feletti betegeknél.
eredmények
Szekvenciális terápia a 7 napos hármas terápiával szemben.
A szekvenciális terápia 22 RCT-n volt hatékonyabb (RR = 1,21, 95% CI: 1,17-1,25). Összesen 2449 szekvenciális terápiában részesülő beteget hasonlítottak össze 2566-tal, akik 7 napos hármas terápiát kaptak, az eradikációs hatékonyság 86,5% (95% CI: 82,9-89,7%), illetve 71,5 (95% CI: 68,4-74,5%). .
Az egyik tanulmány a szekvenciális terápia hatékonyságát a PPI-ket, amoxicillint és metronidazolt, valamint PPI-ket, amoxicillint és klaritromicint alkalmazó hármas terápiával hasonlította össze; a szekvenciális terápia 15,9%-kal, a második 24,0%-kal volt hatékonyabb, mint az első.
Szekvenciális terápia a 10 napos hármas terápiával szemben.
Tizennégy RCT csak csekély eltérést mutatott a szekvenciális eradikációs rendszer hatékonyságában (RR = 1,11, 95% CI: 1,04-1,19).
Összesen 1368 beteget vontak be a vizsgálatba, akiket szekvenciális séma komponenseivel kezeltek, és 1376 beteget, akiknél az eradikációt 10 napos hármas terápiával végezték, a hatásosság 84,3%, illetve 75,3% volt.
Szekvenciális terápia a 14 napos hármas terápiával szemben.
7 vizsgálat eredményei arra utalnak, hogy a két fenti séma összehasonlítása során nincs különbség a hatékonyságban (RR = 1,00, 95% CI: 0,94-1,06).
A szekvenciális terápia hatékonysága 1224 betegnél 80,8%, a 14 napos hármas terápiát alkalmazó betegek csoportjában (n = 1227) pedig 81,3%.
Szekvenciális terápia bizmut alapú kvadroterápia ellen.
3 RCT eredményeinek elemzése nem mutatta ki az egyik eradikációs séma előnyeit a másikkal szemben (RR = 1,01, 95% CI: 0,95-1,06).
Az eradikáció hatékonysága 546 szekvenciális terápiában részesült betegnél 86,2%, a kvadroterápiában szereplő gyógyszerekkel eradikáción átesett 545 betegnél 84,9%.
Szekvenciális terápia a kvadroterápia ellen bizmut gyógyszer nélkül.
Hat RCT hasonlította össze a szekvenciális terápia (n = 1039) és a kvadroterápia (n = 1031) hatékonyságát PPI-k, amoxicillin, klaritromicin és metronidazol alkalmazásával (a terápia időtartama 4 vizsgálatban 10 nap, 2 vizsgálatban 5 nap volt). Az eredmények elemzése azt mutatta, hogy az eradikáció százalékos aránya mindkét sémával azonos volt (81,3% kvadroterápia és 81,7% szekvenciális terápia esetén).
A metaanalízisben nem szereplő tanulmányok eredményei
Szekvenciális terápia versus szekvenciális levofloxacin terápia.
Három vizsgálatban a klaritromicinnel végzett szekvenciális terápia hatékonyságát hasonlították össze a szekvenciális terápiával, amelyben a klaritromicin helyett levofloxacint alkalmaztak napi 500-1000 mg dózisban.
A napi 1000 mg levofloxacint alkalmazó 240 betegnél az eradikáció százalékos aránya 90,0%, a klasszikus klaritromicin szekvenciális terápiában részesült 240 betegnél pedig 78,7% volt a hatásosság. A mellékhatások gyakorisága megközelítőleg azonos volt (24,3%, illetve 24,4%).
A napi 500 mg levofloxacinnal (n = 241) és a klasszikus szekvenciális eradikációs rendszerrel (n = 240) végzett kezelés összehasonlításakor a hatékonyság az első esetben 89,8%, a második esetben pedig 79,5%. A mellékhatások gyakorisága 13,8%, illetve 14,3% volt. Az eredmények elemzése alapján arra a következtetésre jutottunk, hogy a levofloxacint használó szekvenciális eradikációs séma hatékonyabb, mint a klaritromicinnel végzett szekvenciális séma.
A 10 napos és a 14 napos szekvenciális eradikációs sémák összehasonlítása.
Két RCT hasonlította össze a szekvenciális terápia időtartamát: 340 beteg kapott 10 napos szekvenciális terápiát, és 340 beteg kapott 14 napos terápiát. A terápia eredményessége 87,6%, illetve 89,7% volt, ami nem igazolta, hogy a terápia időtartamának növelése növeli annak hatékonyságát.
Következtetés
A metaanalízis eredményei azt mutatják, hogy a Helicobacter pylori fertőzés szekvenciális eradikációs sémája hatékonyabb, mint a 7 napos standard hármas terápia, és hasonló hatékonyságot mutat a 10 napnál hosszabb ideig előírt és 2-nél több antimikrobiális gyógyszert tartalmazó eradikációs sémákkal összehasonlítva. .